Yenka es un software educativo, que permite al usuario realizar simulaciones y crear contenidos de forma sencilla. En esta ocasión, entraremos en la parte química y realizaremos una simulación de un laboratorio en el cual elaboraremos sales.
OBJETIVO:
- Aprender a realizar sales
- Saber de que compuestos se forman las sales
- Aprender a realizar las nomenclaturas para las sales
¿QUE SON SALES?
Una sal es un compuesto químico formado por cationes enlazados a aniones mediante un enlace ionico. Son el producto típico de una reacción química entre una base y un ácido, donde la base proporciona el catión, y el ácido el anión.
Una sal es el producto de la reacción entre un ácido y una base, en esta reacción también se produce agua; en términos muy generales, este tipo de reacción se puede escribir como :
BASE + ÁCIDO→SAL + AGUA
Na
|
| Cl | → | NaCl + | H2O |
Un ejemplo es la sal de mesa, denominada en el lenguaje coloquial sal común, sal marina o simplemente sal. Es la sal específica cloruro de sodio. Su fórmula molecular es NaCl y es el producto de la base hidróxido sódico (NaOH) y ácido clorhídrico (HCl). En general, las sales son compuestos iónicos que forman cristales. Son generalmente solubles en agua, donde se separan los dos iones. Las sales típicas tienen un punto de fusión alto, baja dureza, y baja comprensibilidad. Fundidas o disueltas en agua, conducen la electricidad.
NOMENCLATURA DE LAS SALES
Guiándonos con la nomenclatura tradicional, las sales se denominan con el nombre del anión, seguido de la preposición de y el nombre del catión. Cabe destacar que hay distintos casos como:
- En las sales de hidracidos, se sustituye la terminación -hídrico del hidrácido del que proviene el anión para la terminación -uro. Por ejemplo, NaCl es el cloruro de sodio; el anión Cl- proviene del hidrácido HCl (ácido clorhídrico).
- En las sales de oxoácidos, se sustituye la terminación -oso o-ico del oxoácido del cual proviene el anión por la correspondiente - ito o -ato. Por ejemplo, el Ca3(PO4)2 es el fosfato de calcio; el anión PO43- proviene del H3PO4(ácido fosfórico).
- Las sales ácidas se denominan indicando el número de hidrógenos no sustituidos que quedan en la molécula, usando el prefijo correspondiente. Por ejemplo, el NaHSO es la hidrogenosulfuro de sodio; el anión HS- proviene del ácido sulfhídrico.
- Las sales básicas se nombran indicando el número de hidroxilos seguido del anión central y finalmente el catión. Por ejemplo, el MgCl (OH) es el hidroxicloruro de magnesio.
- Las sales hidratadas se denominan indicando la sal correspondiente y seguidamente el número de moléculas de agua de hidratación.
ELABORACIÓN DE SALES
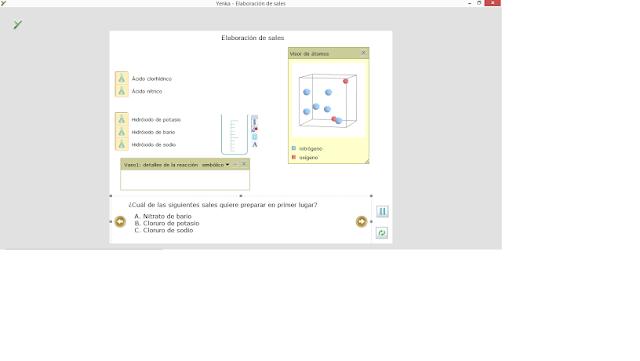







No hay comentarios:
Publicar un comentario